藥廠微生物監控很重要嗎? 需要鑒定每一株菌嗎?
發布時間:2022-08-22 瀏覽次數:2515

藥廠的微生物監控,要從法規開始談起
大家都知菌種鑒定是藥廠微生物監控不可或缺的一環,難道需要監控到一顆菌株都不能出現才算合格嗎?
依據USP<1113>(美國藥典法第1113章節)的規范,微生物監控的重要性是在于:在藥品的制造生產過程中,一旦偵測到菌,必須對其特征/特性有所了解,包括鑒定和菌株分型,進而得知他對成品的危害程度大小。
此外,當執行完整的滅菌步驟后,若仍有受菌污染的狀況發生,此時進行菌種鑒定是很重要的。
不同條件的制造廠有不同規范標準
USP<62>(美國藥典微生物鑒定第62章節)指出,對于不需無菌條件生產產品的制造廠,只需進行特定微生物(致病菌)的測試。
實驗上,只需在選擇性培養基或診斷性培養基上生長且表現出特定型態的菌株進行鑒定需求。
對于需無菌條件生產的藥廠,USP <71>(美國藥典微生物鑒定章節第71章節)提及,若廠內近性標準滅菌流程后,進行無菌測試結果中,仍長出的細菌,可藉由菌種鑒定了解它的特性,從而發現滅菌的材料或技術有什么問題。
USP <1113>(美國藥典微生物鑒定章節第1113章節)敘述中提及:選擇可鑒定到strain-level的鑒定系統,對于污染源的溯源追蹤較合適。
藥廠潔凈等級劃分ABCD級法規要求
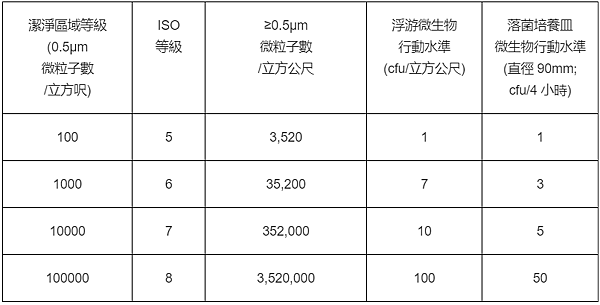
潔凈區域之空氣等級及微生物品質如下表:
空氣等級(國際醫藥品稽查協約組織藥品優良制造準則, PIC/S):
| 靜態 | 動態 | |||
| 等級 | 微粒最大允許量/立方公尺 | |||
| ≥0.5μm | ≥5μm | ≥0.5μm | ≥5μm | |
| A | 3,500 | 1 | 3,500 | 1 |
| B | 3,500 | 1 | 350,000 | 2,000 |
| C | 350,000 | 2,000 | 3,500,000 | 20,000 |
| D | 3,500,000 | 20,000 | 未界定 | 未界定 |
ISO等級5的微粒濃度相等于100級,和歐盟分類的A級潔凈區規范相等。
正常情況下,ISO等級5(A級潔凈區)環境等級區的樣本,應無微生物生長。
A級潔凈區:通常為藥廠高風險無菌操作區域。
B級潔凈區:通常為和A級區相連的走道或區間。
C 、D級潔凈區:無菌要求等級較低的區域,對于菌量的容忍度較高,但不可超標。
USP <1116> 美國藥典微生物鑒定章節<1116>針對分離菌株的微生物鑒定:
? 成功的環境控制須對于所獲取到的微生物菌群進行適當比例的鑒定。
? 菌種鑒定的資訊收集對于調查污染源,尤其是超過環境安全等級規范數量有很大的幫助。
? 關鍵和緊鄰區域的微生物鑒定應優先于非關鍵區域的微生物鑒定。





